2014年上半年以來,我院MBL課題組, 在化學生物傳感與計量學國家重點實驗室主任、2003网站太阳集团和生物學院譚蔚泓教授領導下,在腫瘤靶向藥物和生物成像研究方面取得了系列重大進展,相關成果發表今年在J. Am. Chem. Soc.(美國化學會志),Angew. Chem. Int. Ed.(德國應用化學)這兩個化學學科國際頂級刊物上發表論文八篇。
靶向藥物指的是在細胞分子水平上能夠識别腫瘤組織,從而使腫瘤細胞特異性死亡,而不會波及其他正常細胞的智能型藥物,因此靶向藥物又稱為“生物導彈”。該課題組通過将小分子藥物修飾到核酸适配體上,開發了一種用于靶向治療的核酸适配體-抗癌藥加合物。該系統的靶向治療效果已在老鼠活體試驗中得到了很好的驗證(NPG Asia Materials, 2014, Just accepted)。為了進一步實現核酸适配體-抗癌藥加合物的自動化和模塊化制備,課題組設計和提出了一種通用的合成方法,在DNA/RNA合成儀上實現了核酸适配體-抗癌藥加成物的自動化合成(J. Am. Chem. Soc., 2014, 136, 2731)。除此之外,基于滾壞擴增反應,課題組還提出了一種簡易的方法用于制備核酸适配體共轭的具有FRET(熒光能量共振轉移)功能的納米花(NFs),實現了靶細胞的多元成像和靶向藥物的追蹤輸送,該工作發表在Angew. Chem. Int. Ed.上,并被選為熱點論文(Angew. Chem. Int. Ed., 2014, 53, 5821)。他們還利用DNA核酸适配體特定的構象轉換性質和支點誘導的鍊置換反應,設計了DNA納米爪,實現了對多個癌細胞表面标記物的邏輯檢測、智能診斷和靶向光動力學治療(J. Am. Chem. Soc., 2014, 136, 1256)。
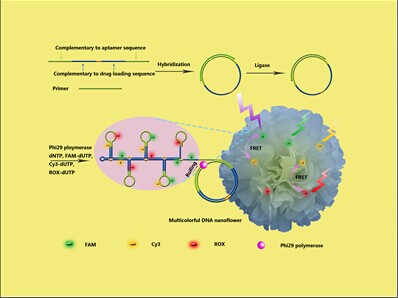
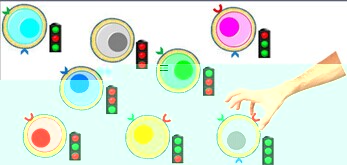
在活細胞生物成像方面,該課題組同樣取得了突破性進展。他們利用脂質體-DNA共轭物在活細胞表面高效自組裝了DNA生物傳感器,實現了對細胞微環境中特定目标物的實時在線檢測分析(J. Am. Chem. Soc., 2014, 136 , 13090)。基于TBET能量轉移機制,課題組開發了一種雙光子熒光探針,實現了對活細胞和組織的比率成像分析(J. Am. Chem. Soc., 2014, 136 , 9838)。利用常見的小分子試劑開發了一種簡易、高效、低成本的方法實現了疏水性磁性顆粒從油相到水相的轉換。該方法有效地解決了疏水性納米顆粒在生物成像和藥物輸送等方面的瓶頸問題(J. Am. Chem. Soc., 2014, 136 12552)。除此之外,他們首次利用表面生長石墨烯的方法成功研制了超級穩定的銀納米顆粒,并通過在表面功能化修飾核酸适配體和炔基分子實現了靶向和低背景拉曼成像(J. Am. Chem. Soc. 2014, 136, 13558)。
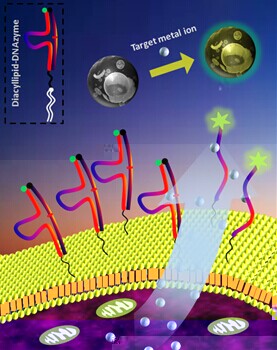

課題組還應邀在化學學科國際頂級綜述類期刊Accounts of Chemical Research發表了關于功能核酸納米材料在細胞傳感、成像及靶向治療等領域的研究進展和應用的綜述論文。與其他綜述性雜志不同,該雜志主要是綜述作者自己的系統研究,該綜述論文的發表表明課題組在腫瘤靶向藥物輸送和活細胞生物成像方面的研究得到了國際同行的高度認可(Accounts of Chemical Research, 2014, 47, 1891)。這些工作的主要研究人員有張曉兵教授, 陳卓教授和葉茂教授和其他課題組人員。
|